Цель — оценка эффективности эзофагопротектора в снижении риска рецидива симптоматики гастроэзофагеальной рефлюксной болезни (ГЭРБ) у пациентов, которым требуется временная отмена терапии ингибиторами протонной помпы (ИПП).
Материал и методы. В проспективное сравнительное исследование селективно были отобраны пациенты, которые длительно (не менее одного месяца) принимали ИПП по поводу основного заболевания и которым требовалась временная отмена антисекреторной терапии ввиду объективных медицинских причин. В исследование были включены пациенты с эндоскопически и/или рН-метрически верифицированной ГЭРБ, а также гистологически верифицированным пищеводом Барретта. В процессе рандомизации пациентов сформированы две равные группы в зависимости от получаемой терапии на время отмены ИПП: первая группа получала антациды в режиме «по требованию», вторая группа — антациды в режиме «по требованию», а также эзофагопротектор Альфазокс в дозе 10 мл четыре раза в сутки (после каждого приема еды и на ночь). Период наблюдения за пациентами составил две недели. Эпизоды изжоги пациенты регистрировали в личных дневниках.
Результаты. В исследование были включены 60 пациентов (28 мужчин и 32 женщины), которым в силу разных причин требовалась отмена ИПП в течение двух недель. Средний возраст обследованных составил 43,1 ± 5,3 года. Было выделено две группы по 30 человек, дифференцированных по методу купирования рецидива изжоги — монотерапия антацидами по требованию или Альфазокс 10 мл четыре раза в день в комбинации с антацидом по требованию. К окончанию двухнедельного периода наблюдения частота рецидива симптоматики в первой группе составила 36,7%, тогда как во второй группе — 13,3%. Применение эзофагопротектора Альфазокса способствовало достоверному регрессу риска рецидива изжоги (отношение шансов 0,2657; 95%-ный доверительный интервал (ДИ) 0,07328–0,9637; p = 0,0438) в сравнении с группой пациентов, которая получала только антациды в режиме «по требованию». При анализе популяции пациентов, у которых произошел рецидив симптоматики, было продемонстрировано, что среднее количество эпизодов изжоги в первой группе составило 6,18 (95% ДИ 4,1930–8,1706), а у пациентов второй группы — 4,50 (95% ДИ 0,7121–8,2879).
Заключение. Настоящее проспективное сравнительное исследование продемонстрировало, что использование эзофагопротектора Альфазокс способствует снижению риска рецидива симптоматики ГЭРБ у пациентов, которым требуется временная отмена терапии ИПП.
Ключевые слова: гастроэзофагеальная рефлюксная болезнь, пищевод Барретта, ингибиторы протонной помпы, эзофагопротектор, Альфазокс
Гастроэзофагеальная рефлюксная болезнь (ГЭРБ) представляет собой чрезвычайно распространенное в мировой популяции кислотозависимое заболевание, при котором соляная кислота желудочного сока выступает основным повреждающим фактором при развитии клинических симптомов и морфологических проявлений [1, 2]. Для данного заболевания характерной чертой является хронический, рецидивирующий паттерн симптоматики, оказывающий существенное негативное влияние на качество жизни больных [3–5]. Текущие эпидемиологические данные свидетельствуют, что показатели распространенности и заболеваемости ГЭРБ имеют неуклонную тенденцию к росту во многих регионах мира [6, 7]. Согласно последнему метаанализу J.S. Nirwan и соавт. (2020), обобщившему результаты 102 исследований, глобальная распространенность ГЭРБ составляет 13,98% (95% доверительный интервал (ДИ) 12,47–15,56%) [8]. Медико-социальное значение ГЭРБ определяется ее главной ролью в развитии предракового состояния, известного как пищевод Барретта (ПБ), при котором специализированный цилиндрический эпителий с бокаловидными клетками замещает нормальный неороговевающий многослойный плоский эпителий дистального отдела пищевода [9, 10]. Согласно недавнему метаанализу L.H. Eusebi и соавт. (2021), обобщившему результаты 44 исследований, частота гистологически верифицированного ПБ у пациентов с ГЭРБ составляет 7,2% (95% ДИ 5,4–9,3%), тогда как эндоскопические признаки ПБ выявляются у 12,0% больных (95% ДИ 5,5–20,3%) [11].
С учетом того что ГЭРБ является классическим кислотозависимым заболеванием, препаратами первой линии при индукции и поддержании ремиссии данной болезни являются ингибиторы протонной помпы (ИПП) [1, 2, 12, 13]. Купирование изжоги в первые сутки применения ИПП у пациентов с ГЭРБ происходит примерно у 31% больных (95% ДИ 0,30–0,32) [14]. При эмпирическом лечении ГЭРБ относительный риск ремиссии изжоги в плацебоконтролируемых исследованиях с использованием ИПП составляет 0,37 (95% ДИ 0,32–0,44) [15]. В метаанализе P.W. Weijenborg и соавт. (2012) терапия ИПП в течение четырех недель приводила к полному купированию изжоги как у пациентов с эрозивной формой заболевания (отношение шансов (ОШ) 0,72; 95% ДИ 0,69–0,74), так и у лиц с неэрозивным фенотипом (ОШ 0,49; 95% ДИ 0,44–0,55) [16]. Вместе с тем с учетом хронического и рецидивирующего течения ГЭРБ после инициального курса ИПП (4–12 недель) для стабильного контроля симптоматики заболевания требуется длительная поддерживающая терапия, которая может назначаться неопределенно долго, повторными курсами, а при наличии ПБ — пожизненно [2, 9, 17]. В клинической практике нередко возникают ситуации, при которых требуется временная (от одной недели до месяца) отмена ИПП для валидного проведения ряда диагностических мероприятий, включая диагностику и контроль эрадикации H. pylori , рН-импедансометрию, а также лабораторный скрининг атрофического гастрита [2, 18, 19]. Отмена ИПП может привести к рецидиву симптоматики у значимой части пациентов, что негативно скажется на их качестве жизни. В ряде исследований частота рецидива при отмене ИПП достигала 60–80% [20–22]. Использование антацидных препаратов для снижения риска рецидива симптоматики на время отмены ИПП малоэффективно ввиду выраженной краткосрочности их действия. В этой связи перспективным представляется оценка эффективности эзофагопротектора Альфазокса, использующегося для формирования макромолекулярного комплекса, обволакивающего слизистую оболочку пищевода и выступающего в качестве механического барьера в отношении соляной кислоты, пепсина и желчных кислот, попадание которых и последующий контакт с эпителием дистального отдела пищевода приводят к индукции симптоматики ГЭРБ [23].
Цель проспективного сравнительного исследования — оценить эффективность эзофагопротектора в снижении риска рецидива симптоматики ГЭРБ у пациентов, которым требуется временная отмена терапии ИПП.
В исследование селективно отбирали пациентов, которые длительно (не менее одного месяца) принимали ИПП по поводу основного заболевания и которым требовалась временная отмена антисекреторной терапии ввиду объективных медицинских причин. Были включены пациенты с эндоскопически и/или рН-метрически верифицированной ГЭРБ, а также гистологически верифицированным ПБ. Пациенты с ПБ и дисплазией высокой степени в исследовании участия не принимали.
В процессе рандомизации пациентов сформировано две равные группы в зависимости от получаемой терапии на время отмены ИПП: первая группа получала антациды в режиме «по требованию»; вторая группа – антациды в режиме «по требованию», а также эзофагопротектор Альфазокс в дозе 10 мл четыре раза в сутки (после каждого приема еды и на ночь). Период наблюдения за пациентами составил две недели. Эпизоды изжоги пациенты регистрировали в личных дневниках.
Статистическую обработку данных проводили с помощью специального программного обеспечения MedCalc 19.7.1 (Бельгия) в среде Microsoft Windows 10 (США). Анализировали такие показатели, как частота рецидива изжоги (в относительном соотношении), кумулятивная частота изжоги (в абсолютном соотношении) и среднее количество эпизодов изжоги на одного пациента за период наблюдения (в абсолютном соотношении). Статистические гипотезы проверяли с помощью непараметрического U-критерия Манна – Уитни и параметрического критерия Фишера. Различия между группами считались достоверными при р < 0,05.
В проспективное сравнительное исследование было включено 60 пациентов (28 мужчин и 32 женщины). Средний возраст обследованных составил 43,1 ± 5,3 года. В нозологической структуре преобладали пациенты с неэрозивной рефлюксной болезнью (n = 32), затем расположились больные эрозивным рефлюкс-эзофагитом (n = 13) и ПБ (n = 15). Основные причины временной отмены антисекреторной терапии с применением ИПП приведены в таблице.
Рис. 1. Частота рецидива симптоматики в группах за период наблюдения
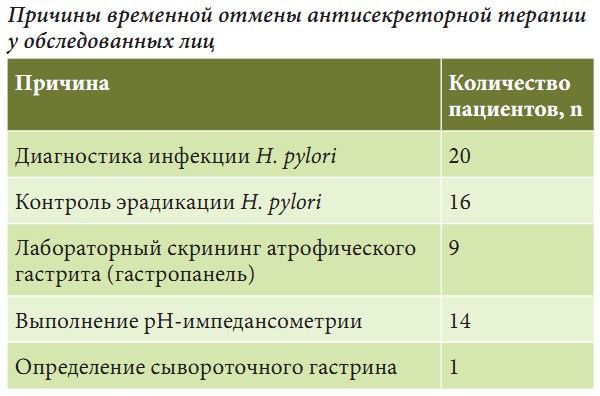
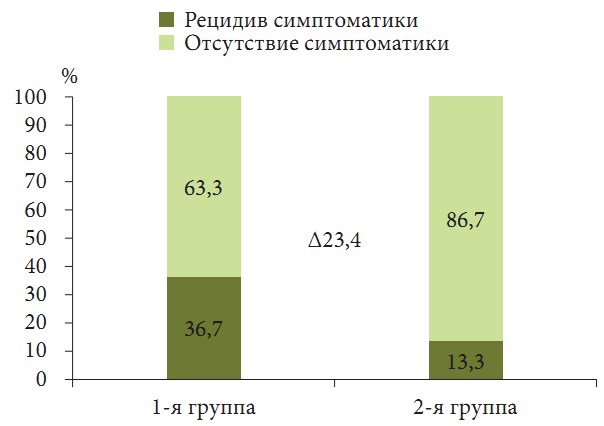
К окончанию двухнедельного периода наблюдения частота рецидива симптоматики в первой группе составила 36,7% (в 11 случаях из 30), тогда как во второй группе – всего в 13,3% (в четырех случаях из 30) (рис. 1). Таким образом, применение эзофагопротектора Альфазокса способствовало достоверному регрессу риска рецидива изжоги (ОШ 0,2657; 95% ДИ 0,07328–0,9637; p = 0,0438) в сравнении с группой пациентов, которая получала только антациды в режиме «по требованию». Кумулятивная частота эпизодов рефлюкса в первой группе составила 68 единиц, а во второй группе — 20 единиц. Анализ популяции пациентов, у которых произошел рецидив симптоматики, показал, что среднее количество эпизодов изжоги в первой группе составило 6,18 (95% ДИ 4,1930–8,1706), а у пациентов второй группы — 4,50 (95% ДИ 0,7121–8,2879) (рис. 2).
Рис. 2. Среднее количество эпизодов изжоги (n) у пациентов с рецидивом симптоматики в группах за период наблюдения
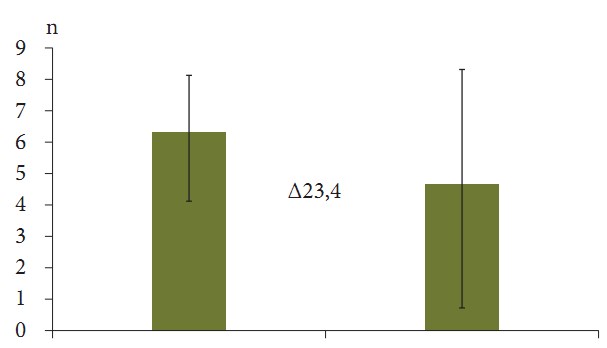
ГЭРБ — широко распространенное кислотозависимое заболевание, развивающееся на фоне первичного нарушения двигательной функции верхних отделов пищеварительного тракта, классическим проявлением которого является изжога [1, 24]. На сегодняшний день антисекреторная терапия с использованием ИПП является терапией первой линии при индукции и поддержании ремиссии ГЭРБ [12, 13, 24–27]. В рутинной клинической практике нередко бывают ситуации, при которых требуется временная (от одной недели до месяца) отмена ИПП для валидного проведения ряда диагностических мероприятий, что может привести к рецидиву симптоматики у значимой части пациентов [2, 18, 19, 21, 22]. Предупреждение рисков рецидива с применением современных групп препаратов является важной задачей современной гастроэнтерологии, так как от его успеха зависит качество жизни пациента — главного интегрального показателя качественной медицинской помощи [2]. Эзофагопротекторы — это новая фармакологическая группа, представителем которой является биоадгезивная формула на основе гиалуроновой кислоты и хондроитина сульфата (Альфазокс), созданная для защиты слизистой оболочки пищевода [1, 23, 28]. Настоящее сравнительное исследование на популяции пациентов, которым требуется временная отмена терапии ИПП, продемонстрировало, что применение эзофагопротектора Альфазокса в сочетании с антацидами способствовало регрессу риска рецидива изжоги.
Представляется, что такая эффективность обусловлена механизмом действия препарата. Так, Альфазокс оказывает заживляющее и восстанавливающее действие по отношению к эпителию пищевода, а благодаря высокой способности к биоадгезии обеспечивает защиту слизистой оболочки органа в течение длительного времени, снижая вероятность контакта соляной кислоты с эпителиоцитами, что необходимо для индукции симптоматики заболевания [23]. Согласно клиническим исследованиям, Альфазокс способствует заживлению эрозий пищевода, в том числе в сочетании с ИПП у пациентов с ГЭРБ [29, 30]. В исследовании V. Savarino и соавт. (2017) комбинация Альфазокса и ИПП позволила более эффективно добиться регрессии клинических проявлений заболевания и улучшения качества жизни пациентов (согласно опроснику SF36) по сравнению с монотерапией ИПП [31]. Полученные в нашем исследовании результаты подтверждают, что оптимизация схем лечения ГЭРБ с использованием эзофагопротекторов открывает новые перспективы ведения этой непростой группы пациентов, в том числе в нетривиальных клинических ситуациях.
Настоящее проспективное сравнительное исследование продемонстрировало, что использование эзофагопротектора Альфазокса способствует снижению риска рецидива симптоматики ГЭРБ у пациентов, которым требуется временная отмена терапии ИПП.
1. Ивашкин В.Т., Маев И.В., Трухманов А.С. и др. Рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению гастроэзофагеальной рефлюксной болезни // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2020. Т. 30. № 4. С. 70–97.
2. Маев И.В., Бусарова Г.А., Андреев Д.Н. Болезни пищевода. М.: ГЭОТАР-Медиа, 2019.
3. Ofman J.J. The economic and quality-of-life impact of symptomatic gastroesophageal reflux disease // Am. J. Gastroenterol. 2003. Vol. 98. № 3. P. 8–14.
4. Maleki I., Masoudzadeh A., Khalilian A., Daheshpour E. Quality of life in patients with gastroesophageal reflux disease in an Iranian population // Gastroenterol. Hepatol. Bed Bench. 2013. Vol. 6. № 2. P. 96–100.
5. Gorczyca R., Pardak P., Pękala A., Filip R. Impact of gastroesophageal reflux disease on the quality of life of Polish patients // World J. Clin. Cases. 2019. Vol. 7. № 12. P. 1421–1429.
6. Chatila A.T., Nguyen M.T.T., Krill T. et al. Natural history, pathophysiology and evaluation of gastroesophageal reflux disease // Dis. Mon. 2020. Vol. 66. № 1. P. 100848.
7. El-Serag H.B., Sweet S., Winchester C.C., Dent J. Update on the epidemiology of gastro-oesophageal reflux disease: a systematic review // Gut. 2014. Vol. 63. № 6. P. 871–880.
8. Nirwan J.S., Hasan S.S., Babar Z.U. et al. Global prevalence and risk factors of gastro-oesophageal reflux disease (GORD): systematic review with meta-analysis // Sci. Rep. 2020. Vol. 10. № 1. P. 5814.
9. Tanţău M., Laszlo M., Tanţău A. Barrett's esophagus – state of the art // Chirurgia (Bucur). 2018. Vol. 113. № 1. P. 46–60.
10. Mohy-Ud-Din N., Krill T.S., Shah A.R. et al. Barrett's esophagus: what do we need to know? // Dis. Mon. 2020. Vol. 66. № 1. P. 100850.
11. Eusebi L.H., Cirota G.G., Zagari R.M., Ford A.C. Global prevalence of Barrett's oesophagus and oesophageal cancer in individuals with gastro-oesophageal reflux: a systematic review and meta-analysis // Gut. 2021. Vol. 70. № 3. P. 456–463.
12. Akiyama J., Kuribayashi S., Baeg M.K. et al. Current and future perspectives in the management of gastroesophageal reflux disease // Ann. NY Acad. Sci. 2018. Vol. 1434. № 1. P. 70–83.
13. Chapelle N., Ben Ghezala I., Barkun A., Bardou M. The pharmacotherapeutic management of gastroesophageal reflux disease (GERD) // Expert Opin. Pharmacother. 2021. Vol. 22. № 2. P. 219–227.
14. McQuaid K.R., Laine L. Early heartburn relief with proton pump inhibitors: a systematic review and meta-analysis of clinical trials // Clin. Gastroenterol. Hepatol. 2005. Vol. 3. № 6. P. 553–563.
15. Sigterman K.E., van Pinxteren B., Bonis P.A. et al. Short-term treatment with proton pump inhibitors, H2-receptor antagonists and prokinetics for gastro-oesophageal reflux disease-like symptoms and endoscopy negative reflux disease // Cochrane Database Syst. Rev. 2010. № 11. CD 002095.
16. Weijenborg P.W., Cremonini F., Smout A.J., Bredenoord A.J. PPI therapy is equally effective in well-defined non-erosive reflux disease and in reflux esophagitis: a meta-analysis // Neurogastroenterol. Motil. 2012. Vol. 24. № 8. P. 747–757.
17. Venkataraman J., Krishnan A. Long-term medical management of gastro-esophageal reflux disease: how long and when to consider surgery? // Trop. Gastroenterol. 2012. Vol. 33. № 1. P. 21–32.
18. Маев И.В., Андреев Д.Н., Кучерявый Ю.А. Диагностика и эрадикационная терапия инфекции Helicobacter pylori: пособие для врачей. Серия Практическая гастроэнтерология. М.: Прима Принт, 2021. 28 с.
19. Тактика врача-гастроэнтеролога: практическое руководство / под ред. акад. РАН И.В. Маева. М.: ГЭОТАР-Медиа, 2021. 312 с.
20. Björnsson E., Abrahamsson H., Simrén M. et al. Discontinuation of proton pump inhibitors in patients on long-term therapy: a double-blind, placebo-controlled trial // Aliment. Pharmacol. Ther. 2006. Vol. 24. № 6. P. 945–954.
21. Schey R., Alla S.P., Midani D., Parkman H.P. Gastroesophageal reflux disease-related symptom recurrence in patients discontinuing proton pump inhibitors for Bravo® wireless esophageal pH monitoring study // Rev. Gastroenterol. Mex. 2017. Vol. 82. № 4. P. 277–286.
22. Hoshikawa Y., Nikaki K., Sonmez S. et al. Exacerbation of gastroesophageal reflux symptoms after discontinuation of proton pump inhibitors is not associated with increased esophageal acid exposure // Neurogastroenterol. Motil. 2020. Vol. 32. № 1. P. e13735.
23. Маев И.В., Андреев Д.Н., Кучерявый Ю.А., Шабуров Р.И. Современные достижения в лечении гастроэзофагеальной рефлюксной болезни: фокус на эзофагопротекцию // Терапевтический архив. 2019. Т. 91. № 8. С. 4–11.
24. Бордин Д.С., Колбасников С.В., Кононова А.Г. Гастроэзофагеальная рефлюксная болезнь: типичные проблемы терапии и пути их преодоления // Доктор.ру. Гастроэнтерология. 2016. Т. 1. № 118. С. 14–18.
25. Лазебник Л.Б., Бордин Д.С., Машарова А.А. и др. Факторы, влияющие на эффективность лечения ГЭРБ ингибиторами протонной помпы // Терапевтический архив. 2012. Т. 84. № 2. С. 16–21.
26. Blackshaw L.A., Bordin D.S., Brock C. et al. Pharmacologic treatments for esophageal disorders // Ann. NY Acad. Sci. 2014. Vol. 1325. № 1. P. 23–39.
27. Бордин Д.С. Как выбрать ингибитор протонной помпы больному ГЭРБ? // Экспериментальная и клиническая гастроэнтерология. 2010. № 2. С. 53–58.
28. Эмбутниекс Ю.В., Валитова Э.Р., Бордин Д.С. Новый подход к лечению гастроэзофагеальной рефлюксной болезни: защита слизистой оболочки пищевода // Эффективная фармакотерапия. 2019. Т. 15. № 18. С. 16–22.
29. Palmieri B., Corbascio D., Capone S., Lodi D. Preliminary clinical experience with a new natural compound in the treatment of esophagitis and gastritis: symptomatic effect // Trends. Med. 2009. Vol. 9. № 4. P. 219–225.
30. Palmieri B., Merighi A., Corbascio D. et al. Fixed combination of hyaluronic acid and chondroitin-sulphate oral formulation in a randomized double blind, placebo controlled study for the treatment of symptoms in patients with non-erosive gastroesophageal reflux // Eur. Rev. Med. Pharmacol. Sci. 2013. Vol. 17. № 24. P. 3272–3278.
31. Savarino V., Pace F., Scarpignato C., Esoxx Study Group. Randomised clinical trial: mucosal protection combined with acid suppression in the treatment of non-erosive reflux disease – efficacy of Esoxx, a hyaluronic acid-chondroitin sulphate based bioadhesive formulation // Aliment. Pharmacol. Ther. 2017. Vol. 45. № 5. P. 631–642.







